内分泌与代谢病学科文献学习系列活动
在目前的基础研究领域中,cGAS-STING pathway正成为一个越来越热门的研究方向。2023年11月1日,内分泌与代谢病学科第148期文献学习系列活动特邀同济大学附属上海市肺科医院刘海鹏研究员,为内分泌科师生开展学术讲座——基于cGAS-STING信号通路的肿瘤靶向干预研究。

刘海鹏研究员及其团队多年来致力于肺部肿瘤与肺部感染的基础和转化研究,以固有免疫分子为切入点,致力于疾病靶标的发现和干预。近年来聚焦于cGAS-STING信号通路,系统阐述了cGAS的多种新型生物学功能及其调控机制,为靶向调控cGAS-STING通路治疗肿瘤和自身免疫性疾病等的临床应用及药物开发提供了重要的理论基础。相关研究结果以第一或通讯作者发表在Nature、Molecular Cell、Nature Communication、Autophagy、EMBO Reports等杂志。授权发明专利4项,参与项目获得教育部自然科学一等奖1项。研究获得国家自然科学基金(5项)、上海市科委、上海市教委等项目资助。
刘海鹏教授首先通过简要介绍免疫反应的基础知识展开了今天的文献学习活动,阐述了免疫反应和肺部疾病(尤其是肺部肿瘤)的关系。
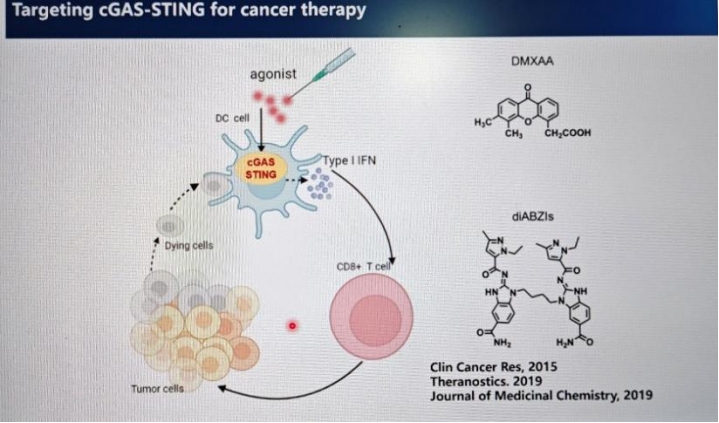
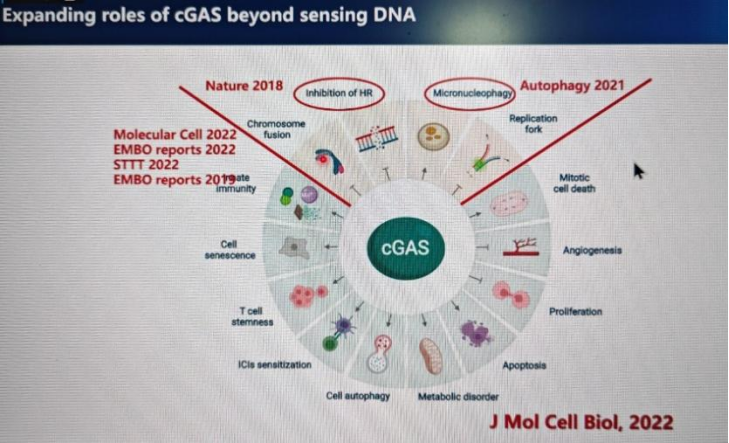
刘教授介绍了cGAS-STING pathway具体通路上的各个分子和反应,包括cGAS的概念、作用以及在不同领域、不同方面所担任的重要角色。
接下来,刘教授介绍了cGAS-STING pathway的经典代谢过程研究。刘教授以铂类药物在肺癌治疗中的化疗抵抗为问题,展开了研究的全面讲解。在基础研究中,刘教授团队发现,cGAS-STING pathway会诱导1型干扰素的生成,从而改善铂类药物引起的化疗抵抗。这一发现给我们在临床上制定不同的肺癌化疗方案带来了启发,Bricanib和platinum结合治疗有望在未来的肺癌治疗中发挥重要作用。在上述研究中,刘教授团队系统阐述了cGAS的多种生物学功能及其调控机制,开发了靶向cGAS-STING信号通路的新的小分子药物,为靶向调控cGAS-STING通路治疗肿瘤和自身免疫性疾病等的临床应用及药物开发提供了重要的理论基础。
另一方面,STING的翻译后修饰目前已有较多研究,刘教授对STING从ER出去的精细过程作了简要介绍。研究发现,STING的活化是TAK1活化所必须的,同时,TAK1对STING的活化也是非常重要且不可或缺的。刘教授团队针对STING和TAK1之间如何互相活化及其相关关系开展基础研究,在讲解中将STING离开ER的过程比喻成船离开码头的过程,生动形象地介绍了STING和TAK1之间的相互关系。
随后,刘教授耐心地解答了陈燕铭教授、石国军主任、朱延华主任、徐芬研究员等老师及各位同学的疑问。
最后,在学科带头人陈燕铭教授的总结中,本次文献学习活动圆满落下帷幕。







