肥胖合并2型糖尿病患者的新希望——减重手术
肥胖症是一种由多因素引起、以脂肪异常蓄积为特征的疾病状态。随着经济发展及生活方式的改变,越来越多的人进入肥胖群体。能量摄入与消耗失衡,导致体内脂肪堆积,是肥胖症发生的基本原因。相较于单纯性肥胖,肥胖合并糖尿病患者的代谢紊乱程度更重,靶器官对胰岛素的敏感性更低,常合并血脂异常,且心血管疾病的发病率显著增加。对于超级肥胖患者而言,传统的治疗方案(饮食、运动、行为控制等)效果不佳。与传统非手术治疗不同,减重代谢手术已经成为肥胖症综合治疗中的一个重要手段,是重度肥胖人群首选的减重治疗方案。
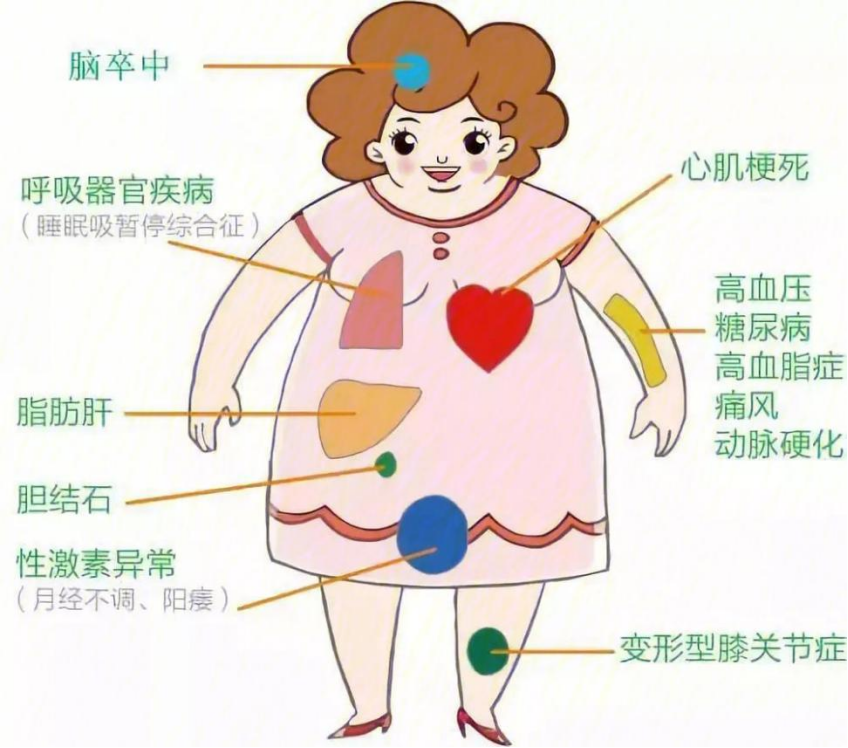
糖尿病是由于胰岛素绝对或相对缺乏,引起糖类、蛋白质和脂肪等代谢异常。血糖长期偏高,容易导致自身内分泌失调,减慢机体新陈代谢,造成脂肪质量增多。且大量研究表明,肥胖与糖尿病严重程度呈正相关。减重手术可以通过重建患者的消化道,减少机体对于食物的摄入和吸收,进而有助于降低体重,改善代谢功能。减重手术是在腹腔镜的辅助下改变胃肠道环境的手术,术后能引起全身脂肪减少(包括外周脂肪和内脏脂肪)。我国肥胖及糖尿病外科治疗指南中指出:对于BMI水平在32.5 kg/m2及以上的患者应积极进行手术治疗,BMI水平在27.5~32.5 kg/m2之间的糖尿病患者可考虑行手术治疗。在减重代谢手术后,由于消化道结构改变、食物摄入减少以及消化吸收减少等因素,患者的体重逐渐减轻,高血糖、高血脂的状态也渐渐改善。此外,脂肪因子谱的改变及氧化应激反应的改善,抑制了胰腺β细胞的凋亡,进而显著改善糖尿病水平。研究表明,β细胞的损伤凋亡与糖尿病病程时间、代谢及血糖控制有关。糖尿病的外科疗效往往更取决于胰腺β细胞的损伤凋亡程度。因此,糖尿病的外科疗效与糖尿病病程时间呈负相关,病程越长则糖尿病缓解率越低。应尽早进行外科治疗,以防病程过长导致手术效果不理想。
2021年《柳叶刀》杂志上发表了一篇长达10年随访的单中心随机对照临床试验,发现超过1/3的减重术后糖尿病患者10年内不需要药物即可将血糖控制在健康水平,并指出在长期控制糖尿病方面,减重手术比药物治疗更佳[1]。研究发现[2],减重手术治疗糖尿病一年有效率可达100%,其完全缓解率高达78%。本研究中术前合并糖尿病患者共22例,其入院平均空腹血糖(9.2±3.2)mmol/L,平均糖化血红蛋白(7.9±1.9)%,其血糖在术后1个月即可达到正常水平,在1年的随访中糖尿病治疗有效率为100%,完全缓解率为91%。
关于减重手术对糖尿病的疗效,众多学者在研究中产生假说:
(1)血清饥饿素(Ghrelin)假说:Ghrelin主要由胃底和近端空肠的X/A样细胞产生并释放,其可刺激下丘脑弓状核的摄食中枢来引导机体启动摄食行为,同时可快速提高血糖,抑制胰岛素的分泌,其分泌异常会造成肥胖和糖尿病[2]。Patel等研究发现[3],减重手术后血清ghrelin水平明显下降,加快胃排空,增加饱腹感,并带来血糖的改善。
(2)小肠假说:为什么不同的术式会对血糖影响不同,根据这个问题出现了两个相互竞争但不相互排斥的竞争学说“前肠学说”和“后肠学说”。前肠假说认为,食物不通过旷置小肠抑制了一种尚不明确的与胰岛素抵抗有关的信号传导或激素分泌,拉杰什也在动物实验中验证了这一假说。后肠学说认为,食物绕过旷置小肠直接进入远端回肠,会增加胰高血糖素肽1和肽YY的分泌,改善β细胞对葡萄糖的敏感性,加快葡萄糖的分解利用,减缓胃排空,降低食欲,促进脂肪分解,从而达到减重降糖作用[4]。
(3)胆汁酸循环假说:减重手术可明显改变患者胆汁酸循环,患者术后胆汁酸水平与葡萄糖水平呈负相关,与胰高血糖素肽1水平呈正相关,从而达到糖尿病的缓解。胆汁酸主要通过法尼酯衍生物X受体、G蛋白偶联胆汁酸受体(TGR5)控制机体的能量代谢和糖脂代谢[5]。McGavigan[6]通过实验对TGR5+/+和TGR5-/-小鼠行减重手术,术后发现血清循环胆汁酸浓度明显增加,胰高血糖素肽1分泌增加,空腹血糖得到改善。同时总结出减重手术术后TGR5信号会加强胆汁酸的代谢,同时对血糖调节做出巨大贡献。
手术是针对肥胖患者的治疗手段之一,多项临床研究表明,减重手术可快速缓解肥胖症患者糖代谢紊乱的相关症状。疗效确切,不易反弹,安全性好,临床获益证据充分,能够让更多肥胖症,尤其是中重度肥胖症患者得到充分的救治。

参考文献:
- Mingrone,Geltrude et al.“Metabolic surgery versus conventional medical therapy in patientswith type 2 diabetes:10-year follow-up of an open-label,single-centre,randomised controlledtrial.”[J].Lancet(London,England)vol.397,10271(2021):293-304.
- Xu G,Song M.Recent advances in the mechanisms underlying the beneficial effects ofbariatric and metabolic surgery[J].Surg Obes Relat Dis.2021;17(1):231-238.
- Patel RT,Shukla AP,Ahn SM,Moreira M,Rubino F.Surgical control of obesity anddiabetes:the role of intestinal vs.gastric mechanisms in the regulation of body weightand glucose homeostasis[J].Obesity(Silver Spring).2014;22(1):159-169.
- Taylor SI,Yazdi ZS,Beitelshees AL.Pharmacological treatment of hyperglycemia intype 2 diabetes[J].Clin Invest.2021;131(2):e142243.
- Affinati AH,Esfandiari NH,Kraftson AT.Bariatric Surgery in the Treatment of Type 2Diabetes[J].Curr Diab Rep.2019;19(12):156.
- improvements after vertical sleeve gastrectomy in mice[J].Gut.2017;66(2):226-234.McGavigan AK,Garibay D,Henseler ZM,et al.TGR5 contributes to glucoregulatory







